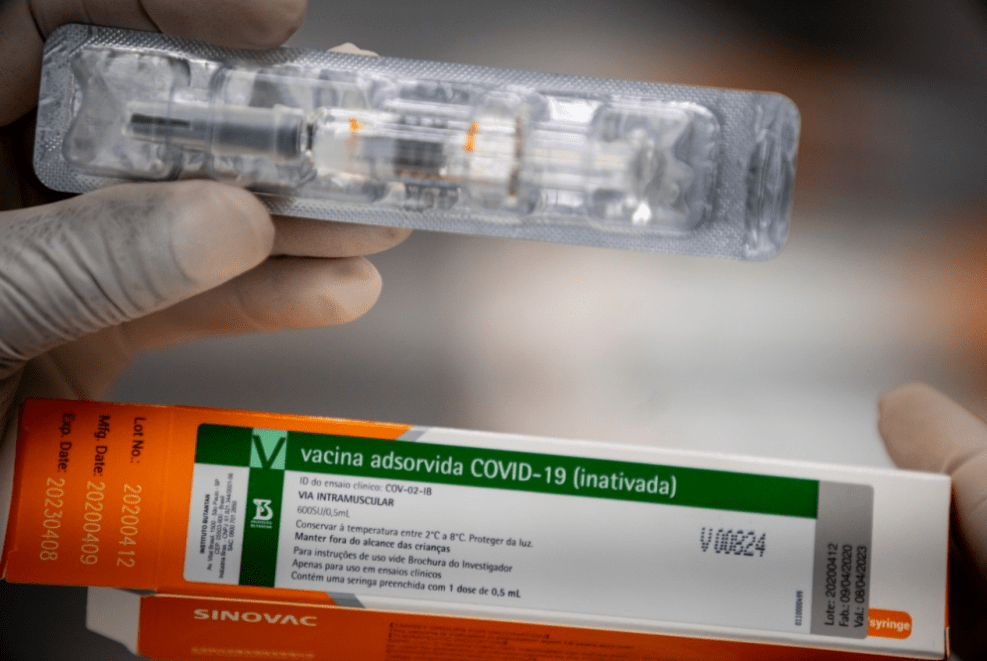
A Anvisa (Agência Nacional de Vigilância Sanitária) aprovou neste domingo (17) o uso emergencial da CoronaVac, vacina desenvolvida pelo Instituto Butantan em parceria com o o laboratório chinês Sinovac. Até o momento, três diretores da Anvisa votaram favoravelmente ao uso emergencial das vacinas. A decisão passa a valer a partir do momento que a ata da reunião for publicada.
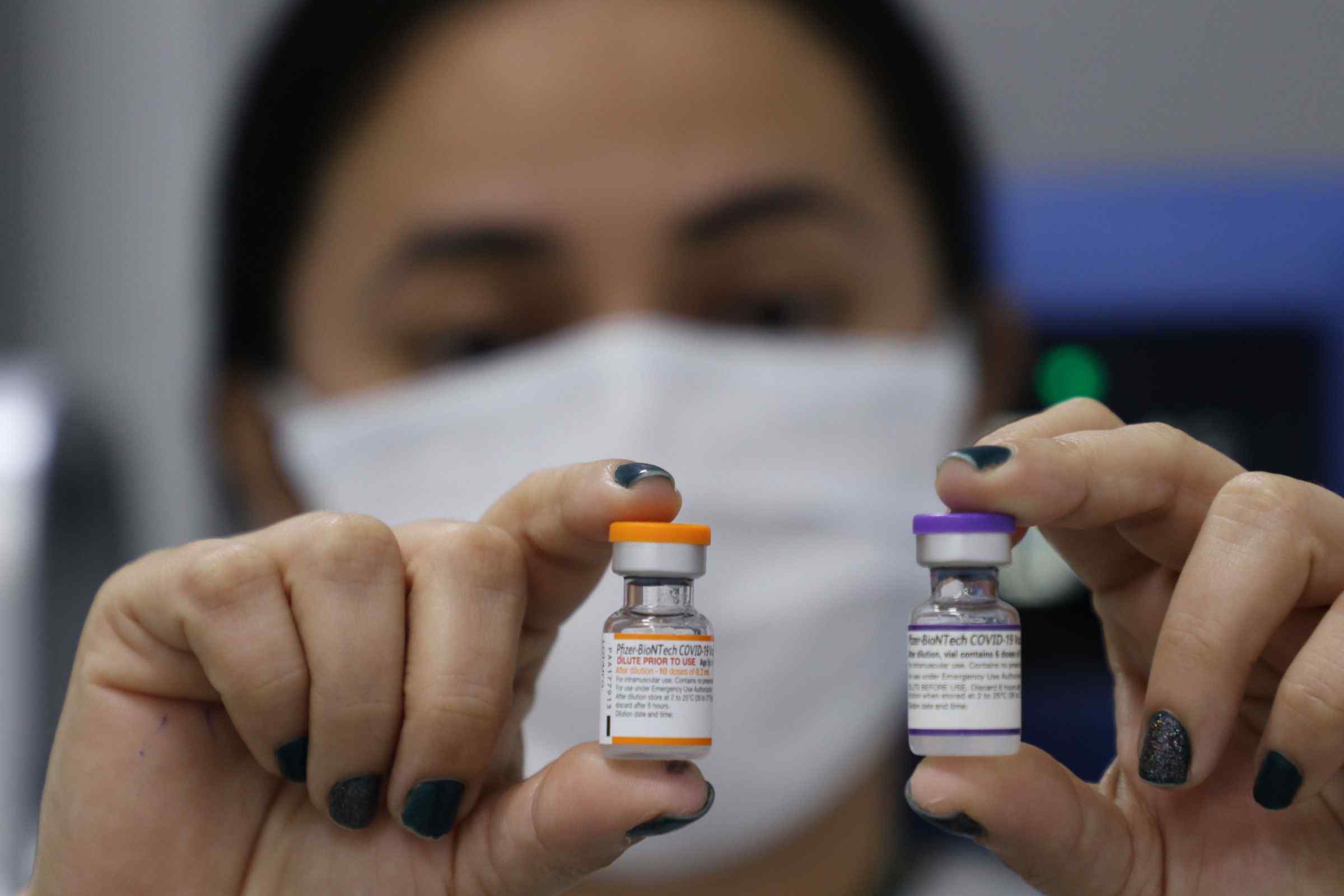
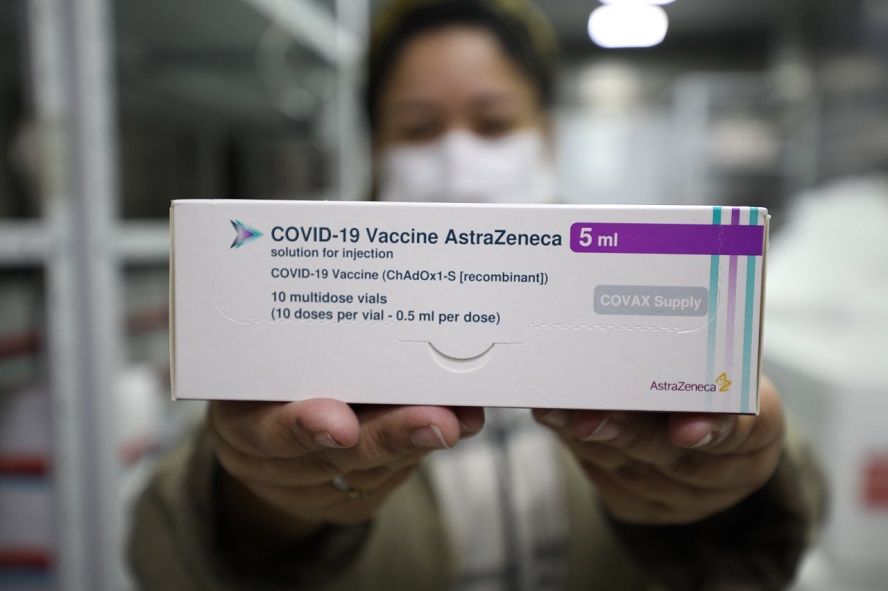
A CoronaVac foi testada em diversos centros de pesquisa no País, entre eles o Hospital das Clínicas de Ribeirão Preto). Também foi aprovada a vacina de Oxford, desenvolvida em conjunto com o laboratório AstraZeneca e que conta com parceria com a Fiocruz (Fundação Oswaldo Cruz).
Durante a reunião, que começou às 10h e foi transmitida pelas plataformas digitais da Anvisa, a gerência-geral de Medicamentos da Anvisa recomendou a aprovação do uso do imunizante, condicionada a reavaliação periódica.

A diretora da Anvisa Meiruze Freitas, relatora dos pedidos de autorização para uso emergencial das vacinas, votou favorável para liberação emergencial dos imunizantes, por considerar que elas são eficazes para prevenir a covid-19.
De acordo com o ministério da Saúde, a campanha de vacinação deve começar já no próximo dia 20 de janeiro, quando as doses começarão a ser entregues nos municípios.
Ainda neste domingo, o governador João Doria (PSDB), vai ser pronunciar no Hospital das Clínicas sobre a decisão da Anvisa. De acordo com o jornal Folha de S. Paulo, o governo estadual deve iniciar ainda neste domingo a vacinação, de forma simbólica.